بفر محلول
ایک بفر محلول (زیادہ واضح طور پر پی ایچ pH بفر یا ہائیڈروجن آئن بفر) ایک تیزابی یا اساسی آبی محلول ہوتا ہے جس میں ایک کمزور تیزاب اور اس کے جوڑی کے اساس کا مرکب ہوتا ہے یا اس کے برعکس ایک کمزور اساس اور اس کے جوڑی کے تیزاب کا مرکب ہوتا ہے۔ [1] جب اس میں تھوڑی مقدار میں مضبوط تیزاب یا اساس ڈالا جاتا ہے تو اس کا پی ایچ pH بہت کم تبدیل ہوتا ہے۔ بفر محلولوں کا استعمال مختلف قسم کے کیمیائی اطلاقات میں pH کو تقریباً مستقل قیمت پر رکھنے کے ایک ذریعہ کے طور پر کیا جاتا ہے۔ فطرت میں، بہت سے زندہ نظام موجود ہیں جو پی ایچ pH کی باقاعدگی کے لیے بفرنگ کا استعمال کرتے ہیں۔ مثال کے طور پر، بائی کاربونیٹ بفرنگ سسٹم خون کے pH کو منظم کرنے کے لیے استعمال کیا جاتا ہے اور بائی کاربونیٹ سمندر میں بفر کے طور پر بھی کام کرتا ہے۔
بفرنگ کے اصول[ترمیم]

کمزور تیزاب +HA اور اس کے جوڑی کے اساس -A کے کیمیائی توازن کی وجہ سے پی ایچ pH میں تبدیلی کے خلاف مزاحمت کرتے ہیں۔
کے درمیان کیمیائی توازن کی وجہ سے بفر سلوشنز pH کی تبدیلی کے خلاف مزاحمت کرتے ہیں۔
جب کمزور تیزاب اور اس کے جوڑی دار اساس کے توازن کے مرکب میں کچھ مضبوط تیزاب شامل کیا جاتا ہے، تو ہائیڈروجن آئنز (+H) شامل کیے جاتے ہیں اور لی شیتیلے Le Chatelier کے اصول کے مطابق توازن بائیں طرف منتقل ہو جاتا ہے۔ اس کی وجہ سے، ہائیڈروجن آئن کا ارتکاز مضبوط تیزاب کی مقدار کے لیے متوقع مقدار سے کم بڑھتا ہے۔اسی طرح، اگر مرکب میں مضبوط الکلی شامل کی جاتی ہے، تو ہائیڈروجن آئن کا ارتکاز اس مقدار سے کم ہو جاتا ہے جو الکلی کی مقدار کے لیے متوقع ہوتا ہے۔ شکل 1 میں، اثر کو .4.7 = pKa کے ساتھ ایک کمزور تیزاب کے مصنوعی ٹائٹریشن سے دکھایا گیا ہے۔ غیر حل شدہ تیزاب کا متعلقہ ارتکاز نیلے رنگ میں دکھایا گیا ہے اور اس کے جوڑی دار اساس کو سرخ میں دکھایا گیا ہے۔ پی ایچ pH، پی ایچ بفر ریجن میں نسبتاً آہستہ آہستہ تبدیل ہوتا ہے،
pH= pKa ± 1
جو 4.7 =pH پر ٹھہر جاتا ہے،
جہاں [-A] = [HA]۔
ہائیڈروجن آئن کا ارتکاز متوقع مقدار سے کم ہو جاتا ہے کیونکہ زیادہ تر اضافی ہائیڈرو آکسائیڈ آئن تعمل میں استعمال ہوجاتا ہے۔
اور +H آئن نیوٹرلائزیشن کے عمل میں صرف تھوڑا استعمال ہوتا ہے (جو وہ تعمل ہے جس کے نتیجے میں پی ایچ میں اضافہ ہوتا ہے)۔
ایک بار جب تیزاب 95 فیصد سے زیادہ ڈیپروٹونیٹ ہو جاتا ہے تو پی ایچ تیزی سے بڑھتا ہے کیونکہ زیادہ تر شامل الکلی نیوٹرلائزیشن ری ایکشن میں استعمال ہوجاتی ہے۔
بفر کی گنجائش[ترمیم]
بفر کی گنجائش تیزاب یا الکلی کے ارتکاز کی تبدیلی کے سلسلے میں بفرنگ ایجنٹ پر مشتمل محلول کے pH کی تبدیلی کے خلاف مزاحمت کا ایک مقداری پیمانہ ہے۔ اس کی تعریف اس طرح کی جا سکتی ہے: [2]
جہاں اضافی بنیاد کی ایک لامحدود طور پر کم مقدار ہے یا
جہاں اضافی تیزاب کی ایک لامحدود طور پر کم مقدار ہے۔ pH کی تعریف −log 10 [H + ] کے طور پر کی گئی ہے اور
d (pH)، پی ایچ pH میں ایک لامحدود طور پر کم تبدیلی ہے۔
میں ایک لامحدود تبدیلی ہے۔
کسی بھی تعریف کے ساتھ ایک کمزور تیزاب HA کے لیے بفر کی صلاحیت کو انحطاط مستقل Ka کے طور پر ظاہر کیا جا سکتا ہے۔ [3] [4]
جہاں [+H] ہائیڈروجن آئنوں کا ارتکاز ہے اور شامل ایسڈ کا کل ارتکاز ہے۔ Kw پانی کی خود آئنائزیشن کے لیے توازن مستقل ہے، جو
x1.0 × 10−14 کے برابر ہے۔ نوٹ کریں کہ محلول میں +H ہائیڈرونیم آئن +H3O کے طور پر موجود ہے اور ہائیڈرونیم آئن کی مزید پانی ملانے کا انحراف کے توازن پر نہ ہونے کے برابر اثر پڑتا ہے، سوائے بہت زیادہ تیزابیت کے۔

یہ مساوات ظاہر کرتی ہے کہ بڑھی ہوئی بفر صلاحیت کے تین علاقے ہیں (شکل 2 دیکھیں)۔
- وکر کے مرکزی علاقے میں (پلاٹ پر سبز رنگ)، دوسری مدت غالب ہے اور بفر کی گنجائش، ایک مقامی زیادہ سے زیادہ (pKa =pH) تک بڑھ جاتی ہے۔ اس چوٹی کی اونچائی pKa کی قدر پر منحصر ہے۔ بفر کی گنجائش اس وقت نہ ہونے کے برابر ہوتی ہے جب بفرنگ ایجنٹ کا ارتکاز [HA] بہت کم ہوتا ہے اور بفرنگ ایجنٹ کے بڑھتے ہوئے ارتکاز کے ساتھ بڑھ جاتا ہے۔ کچھ مصنفین بفر صلاحیت کے گراف میں صرف اس خطے کو دکھاتے ہیں۔ [2] بفر کی گنجائش، زیادہ سے زیادہ کے 33 فیصد تک گرجاتی ہے جب pH = p K a ± 1 اور 10 فیصد تک گرتی ہے جب pH = p K a ± 1.5 اور اور pH = p K a ± 2 پر 1 فیصد تک گر جاتی ہے۔ اس وجہ سے سب سے زیادہ مفید رینج تقریبا 1± pKa ہے۔ کسی مخصوص پی ایچ پر استعمال کے لیے بفر کا انتخاب کرتے وقت، اس کی pKa قدر اس pH کے جتنا ممکن ہو قریب ہونی چاہیے۔ [2]
- تیزابیت والے محلول کے ساتھ، pH تقریباً 2 سے کم (پلاٹ پر رنگین سرخ)، مساوات میں پہلی مدت غالب رہتی ہے اور کم ہوتے ہوئے پی ایچ کے ساتھ بفر کی صلاحیت تیزی سے بڑھ جاتی ہے: اس کا نتیجہ یہ نکلتا ہے کہ دوسری اور تیسری مدت بہت کم پی ایچ پر نہ ہونے کے برابر ہو جاتی ہیں۔ یہ مدت بفرنگ ایجنٹ کی موجودگی یا غیر موجودگی سے آزاد ہے۔
- طاقتور اساسی محلولوں کے ساتھ، pH تقریباً 12 سے زیادہ (پلاٹ پر نیلے رنگ کا)، مساوات میں تیسری مدت غالب رہتی ہے اور بفر کی صلاحیت تیزی سے بڑھتی ہوئی پی ایچ کے ساتھ بڑھ جاتی ہے: اس کا نتیجہ یہ نکلتا ہے کہ پہلی اور دوسری مدت پر بہت زیادہ پی ایچ پر نہ ہونے کے برابر ہو جاتی ہیں۔ یہ اصطلاح بفرنگ ایجنٹ کی موجودگی یا غیر موجودگی سے بھی آزاد ہے۔
بفر محلول کے اطلاقات[ترمیم]
بفرنگ ایجنٹ پر مشتمل محلول کا pH صرف ایک بہت معمولی حد میں مختلف ہو سکتا ہے، قطع نظر اس کے کہ محلول میں اور کیا شامل ہے۔ حیاتیاتی نظاموں میں یہ خامروں کے صحیح طریقے سے کام کرنے کے لیے ایک لازمی شرط ہے۔ مثال کے طور پر، انسانی خون میں کاربونک ایسڈ H2CO3 اور بائی کاربونیٹ (HCO3) کا مرکب پلازما فریکشن میں موجود ہے؛ یہ خون کے pH کو 7.35 اور 7.45 کے درمیان برقرار رکھنے کا اہم طریقہ کار ہے۔ اس تنگ رینج (7.40 ± 0.05 pH یونٹ) سے باہر، تیزابیت اور الکالوسس میٹابولک حالات تیزی سے نشو و نما پاتے ہیں، اگر صحیح بفرنگ کی صلاحیت کو تیزی سے بحال نہ کیا جائے تو بالآخر موت کا باعث بنتی ہے۔
اگر کسی محلول کی pH قدر بڑھ جاتی ہے یا بہت زیادہ گر جاتی ہے تو، ایک عمل میں ایک انزائم کی تاثیر کم ہو جاتی ہے، جسے ڈینیچریشن کہا جاتا ہے، جو عام طور پر ناقابل واپسی ہوتا ہے۔ [5] تحقیق میں استعمال ہونے والے حیاتیاتی نمونوں کی اکثریت کو بفر محلول میں رکھا جاتا ہے، اکثر فاسفیٹ بفرڈ نمکین (PBS) pH 7.4 پر۔
صنعت میں، بفرنگ ایجنٹوں کو تخمیر کے عمل میں استعمال کیا جاتا ہے اور کپڑوں کی رنگائی میں استعمال ہونے والے رنگوں کے لیے موزوں حالت میں لانے کے لیے استعمال کیا جاتا ہے۔ وہ کیمیائی تجزیہ [4] اور پی ایچ میٹر کی نشانزدگی میں بھی استعمال ہوتے ہیں۔
سادہ بفرنگ ایجنٹس[ترمیم]
بفرنگ ایجنٹ pKa مفید pH رینج سائٹرک ایسڈ 3.13، 4.76، 6.40 2.1–7.4 ایسیٹک ایسڈ 4.8 3.8–5.8 KH2PO4 7.2 6.2–8.2 CHES 9.3 8.3–10.3 بوریٹ 9.24 8.25–10.25
تیزابی علاقوں میں بفروں کے لیے، مخصوص بفرنگ ایجنٹ میں ایک مضبوط تیزاب جیسے ہائیڈروکلورک ایسڈ شامل کرکے pH کو مطلوبہ قدر میں ایڈجسٹ کیا جا سکتا ہے۔ الکلائن بفرز کے لیے، سوڈیم ہائیڈرو آکسائیڈ جیسی مضبوط اساس شامل کی جا سکتی ہے۔ متبادل طور پر، ایک تیزاب اور اس کے جوڑی کے اساس کے مرکب سے بفر آمیزہ بنایا جا سکتا ہے۔ مثال کے طور پر، ایک ایسیٹیٹ بفر ایسیٹک ایسڈ اور سوڈیم ایسیٹیٹ کے مرکب سے بنایا جا سکتا ہے۔ اسی طرح، ایک الکلین بفر ایک اساس اور اس کے جوڑی کے تیزاب کے مرکب سے بنایا جا سکتا ہے۔
"آفاقی" بفر آمیزہ[ترمیم]
مادوں کو جن کی pKa قدر صرف دو یا اس سے کم ہوتی ہے کو ساتھ ملاکر اور pH کو ایڈجسٹ کر کے، بفروں کی ایک وسیع رینج حاصل کی جا سکتی ہے۔ سائٹرک ایسڈ بفر مرکب کا ایک مفید جز ہے کیونکہ اس میں تین pKa اقدار ہیں، جو دو سے کم سے فرق رکھتی ہیں۔ بفر رینج کو دوسرے بفرنگ ایجنٹوں کو شامل کرکے بڑھایا جا سکتا ہے۔ مندرجہ ذیل مرکبات (McIlvaine's buffers محلولوں) میں pH کی بفر رینج ہوتی ہے۔ 3 سے 8۔
0.2 0.2 M M Na 2 HPO4 (mL)
0.1 ایم سائٹرک ایسڈ (ایم ایل) پی ایچ 20.55 79.45 3.0 38.55 61.45 4.0 51.50 48.50 5.0 63.15 36.85 6.0 82.35 17.65 7.0 97.25 2.75 8.0
سائٹرک ایسڈ، مونوپوٹاشیم فاسفیٹ، بورک ایسڈ اور ڈائیتھائل باربیٹورک ایسڈ پر مشتمل ایک مرکب پی ایچ کی حد 2.6 سے 12 تک کا احاطہ کرنے کے لیے بنایا جا سکتا ہے۔ [6]
دیگر عالمگیر بفر کارموڈی بفر اور برٹن – رابنسن بفر ہیں، جو 1931 میں تیار ہوئے۔
حیاتیات میں استعمال ہونے والے عام بفر مرکبات[ترمیم]
مؤثر حد کے لیے اوپر بفر کی گنجائش دیکھیں۔ بائیو کیمیکل ایپلی کیشنز میں ان بفر مادوں کے تاریخی ڈیزائن کے اصولوں اور سازگار خصوصیات کے لیے گڈز بفرز بھی دیکھیں۔
| عام نام (کیمیائی نام) | ساخت | pKa 25 °C |
Temp. effect, dpH/dT (K−1)[7] |
مولیکیولر وزن |
|---|---|---|---|---|
| ٹی اے پی ایس ، ([ٹرِس(ہائیڈروکسیمیتھائل)میتھیلامینو]پروپین سلفونک ایسڈ) |
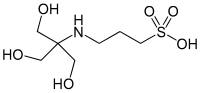
|
8.43 | −0.018 | 243.3 |
| بائیسین ، (2-(bis(2-hydroxyethyl) امینو) acetic acid) |

|
8.35 | −0.018 | 163.2 |
| ٹریس ، (tris(hydroxymethyl) امینو میتھین یا 2-امائنو-2- (ہائیڈروکسی میتھائل) پروپین-1,3-ڈائیول) |

|
8.07[ا] | 0.028- | 121.14 |
| Tricine ، (N-[tris(hydroxymethyl)methyl]glycine) |

|
8.05 | 0.021- | 179.2 |
| TAPSO ، (3-[N-tris(hydroxymethyl)methylamino]-2-hydroxypropanesulfonic acid) |

|
7.635 | 259.3 | |
| HEPES ، (4- (2-ہائیڈروکسیتھائل) -1-پائپرازینیتھینی سلفونک ایسڈ) |

|
7.48 | -0.014 | 238.3 |
| ٹی ای ایس ، (2-[[1,3-dihydroxy-2-(hydroxymethyl)propan-2-yl]amino]ethanesulfonic acid) |
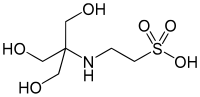
|
7.40 | -0.020 | 229.20 |
| MOPS ، (3- (N-morpholino)پروپین سلفونک ایسڈ) |

|
7.20 | -0.015 | 209.3 |
| پائپس ، (piperazine-N,N′-bis(2-ethanesulfonic ایسڈ)) |
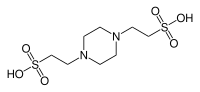
|
6.76 | -0.008 | 302.4 |
| کیکوڈیلیٹ ، (dimethylarsenic ایسڈ) |
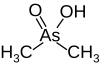
|
6.27 | 138.0 | |
| ایم ای ایس ، (2- (N-morpholino) ایتھین سلفونک ایسڈ) |
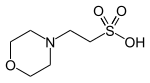
|
6.15 | -0.011 | 195.2 |
مزید دیکھیے[ترمیم]
حوالہ جات[ترمیم]
- ↑ J. Gordon Betts۔ "Inorganic compounds essential to human functioning"۔ Anatomy and Physiology۔ OpenStax۔ ISBN 978-1-947172-04-3۔ اخذ شدہ بتاریخ 14 مئی 2023
- ^ ا ب پ Douglas A. Skoog، Donald M. West، F. James Holler، Stanley R. Crouch (2014)۔ Fundamentals of Analytical Chemistry (9th ایڈیشن)۔ Brooks/Cole۔ صفحہ: 226۔ ISBN 978-0-495-55828-6
- ↑ J. N. Butler (1998)۔ Ionic Equilibrium: Solubility and pH calculations۔ Wiley۔ صفحہ: 133–136۔ ISBN 978-0-471-58526-8
- ^ ا ب A. Hulanicki (1987)۔ Reactions of acids and bases in analytical chemistry۔ ترجمہ بقلم Mary R. Masson۔ Horwood۔ ISBN 978-0-85312-330-9
- ↑ R. Scorpio (2000)۔ Fundamentals of Acids, Bases, Buffers & Their Application to Biochemical Systems۔ ISBN 978-0-7872-7374-3
- ↑ J. Mendham، R. C. Denny، J. D. Barnes، M. Thomas (2000)۔ "Appendix 5"۔ Vogel's textbook of quantitative chemical analysis (5th ایڈیشن)۔ Harlow: Pearson Education۔ ISBN 978-0-582-22628-9
- ↑ "Buffer Reference Center"۔ Sigma-Aldrich۔ 17 اپریل 2009 میں اصل سے آرکائیو شدہ۔ اخذ شدہ بتاریخ 17 اپریل 2009




![{\displaystyle \beta \approx 2.303{\frac {T_{{\ce {HA}}}K_{a}[{\ce {H+}}]}{(K_{a}+[{\ce {H+}}])^{2}}}.}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ec0e3ba9d065bfb822350b58e375d1f4630c6235)

