پانی میں حل پذیری
کسی دھات اور تیزاب کے عمل سے نمکیات بنتے ہیں۔ زیادہ تر نمکیات پانی میں حل ہو جاتے ہیں لیکن ہر نمک پانی میں حل نہیں ہو سکتا۔ کسی نمک کی پانی میں حل پذیری یاد رکھنے کے لیے ابتدائی کیمسٹری کے طالب علموں کو یہ اصول بتائے جاتے ہیں:
- اصول نمبر 1--سوڈیئم، پوٹاشیئم اور امونیئم کے سارے نمکیات پانی میں حل ہو جاتے ہیں۔
- اصول نمبر 2--سارے نائیٹریٹ، اسیٹیٹ اور پرکلوریٹ پانی میں حل ہو جاتے ہیں۔
- اصول نمبر 3--چاندی، سیسے اور پارے1 کے نمک پانی میں حل نہیں ہو سکتے۔ (سوائے نائیٹریٹ، اسیٹیٹ اور پرکلوریٹ کے۔ دیکھیں اصول نمبر 2 )
- اصول نمبر 4-- سارے کلورائیڈ، برومائیڈ اور آیوڈائیڈ پانی میں حل ہو جاتے ہیں۔ ( سوائے چاندی، سیسے اور پارے کے۔ دیکھیں اصول نمبر 3 )
- اصول نمبر 5-- سارے کاربونیٹ، سلفائیڈ، آکسائیڈ اور ہائیڈروآکسائیڈ پانی میں حل نہیں ہوتے۔ (سوائے سوڈیئم، پوٹاشیئم اور امونیئم کے۔ دیکھیں اصول نمبر 1 )
- اصول نمبر 6-- سارے سلفیٹ پانی میں حل ہو جاتے ہیں سوائے بیریئم اور اسٹرونشیئم کے۔ کیلشیئم سلفیٹ کی بہت معمولی مقدار پانی میں حل ہو جاتی ہے۔
درجہ حرارت کا اثر[ترمیم]
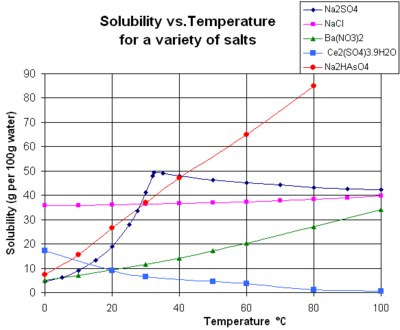
- وہ نمکیات جو پانی میں حل ہونے پر ٹھنڈک پیدا کرتے ہیں ان کی حل پذیری گرم پانی میں بڑھ جاتی ہے جیسے قلمی شورہ یعنی پوٹاشیئم نائیٹریٹ، سوڈیئم آرسینیٹ۔
- وہ نمکیات جنہیں پانی میں حل کرنے سے پانی گرم ہو جاتا ہے ان کی حل پذیری ٹھنڈے پانی میں بڑھ جاتی ہے جیسے ان بجھا چونا، سیریئم سلفیٹ۔
گیسوں کی حل پذیری[ترمیم]
گیسوں کی پانی میں حل ہونے کی صلاحیت پانی گرم کرنے سے کم ہوتی چلی جاتی ہے۔ یہی وجہ ہے کہ پیپسی اور کوکا کولا جیسے مشروبات اگر ٹھنڈے نہ ہوں اور ڈھکن کھول دیا جائے تو بے ذائقہ ہو جاتے ہیں کیونکہ اُن میں موجود کاربن ڈائی آکسائیڈ ضائع ہو جاتی ہے۔
ابالنے سے پانی میں موجود اکثر گیسیں مکمل طور پر پانی سے باہر نکل آتی ہیں مگر ہائیڈروجن کے ہیلائیڈ (فلورائیڈ، کلورائیڈ، برومائیڈ،آیوڈائیڈ) پانی سے مکمل طور پر خارج نہیں ہوتے کیونکہ وہ پانی کے ساتھ ایزیوٹروپ بنا لیتے ہیں۔
صفر درجہ سینٹی گریڈ اور ایک ایٹموسفیئر کے دباو پر ہر ایک ملی لیٹر (ml) پانی میں درج ذیل ملی لیٹر مقدار میں یہ گیسیں حل ہوتی ہیں۔
| گیس کا نام | حل ہونے والی مقدار |
|---|---|
| امونیا | 1300ml |
| ہائیڈروجن کلورائیڈ | 500ml |
| سلفر ڈائی آکسائیڈ | 80ml |
| کاربن ڈائی آکسائیڈ | 1.7ml |
| ethene | 0.25ml |
| آکسیجن | 0.049ml |
| نائیٹروجن | 0.024ml |
نائیٹروجن کی پانی میں حل پذیری تو کم ہے لیکن ہوا میں اس کی مقدار زیادہ ہے (لگ بھگ 80%)۔ یہی وجہ ہے کہ سمندر اور جھیل دریاوں کے پانی میں حل شدہ نائیٹروجن کی مقدار آکسیجن کی دو گنا ہوتی ہے۔
مزید دیکھیے[ترمیم]
حوالہ جات[ترمیم]
- [1]آرکائیو شدہ (Date missing) بذریعہ csudh.edu (Error: unknown archive URL)
